知識分享
減少卵母細胞體積可提高減數分裂停滯精子顯微注射後之活產率
文/茂盛醫院生殖中心研究員張智瑩、陳建宏
目前在臨床上不孕症患者有10%至15%是受無精症影響,通常可以透過開刀取精的方式自睪丸或輸精管獲得完成減數分裂之成熟精子,並藉由細胞質內精子顯微注射 (intracytoplasmic sperm injection, ICSI) 達到受精的目的。而無精症又可分為阻塞型(obstructive azoospermia)與非阻塞型無精症(non-obstructive azoospermia, NOA),其中NOA約佔案例之60%,此類患者可成功獲取精子的機率較低,通常是由於原發性睾丸功能障礙所導致[1]。在NOA患者採集的樣本中約一半無法採集到成熟精子,僅可發現已完成減數分裂但尚未變形之圓形精子細胞(Round sperm)。針對此情形,目前臨床上已研發出使用圓形精子細胞進行注射(round sperm injection, ROSI)之技術並有活產的紀錄,但ROSI過程中,因
正確分辨Round sperm的困難度較高(圖一),故其成功率相對較低。
根據2021年發表之文獻統計,ROSI的受精率為38.7%,妊娠率為3.7%,最終胚胎移植後活產率僅為4.3%,與常規ICSI出生率(36.5%)相比明顯低很多[2]。至目前為止,經ROSI出生嬰兒與經ICSI或傳統IVF出生者相比,尚未發現表徵上有明顯異常,但在ROSI胎兒中可發現了一些遺傳變異,須要進一步的研究來證明與解決該變異誘導畸形之風險。
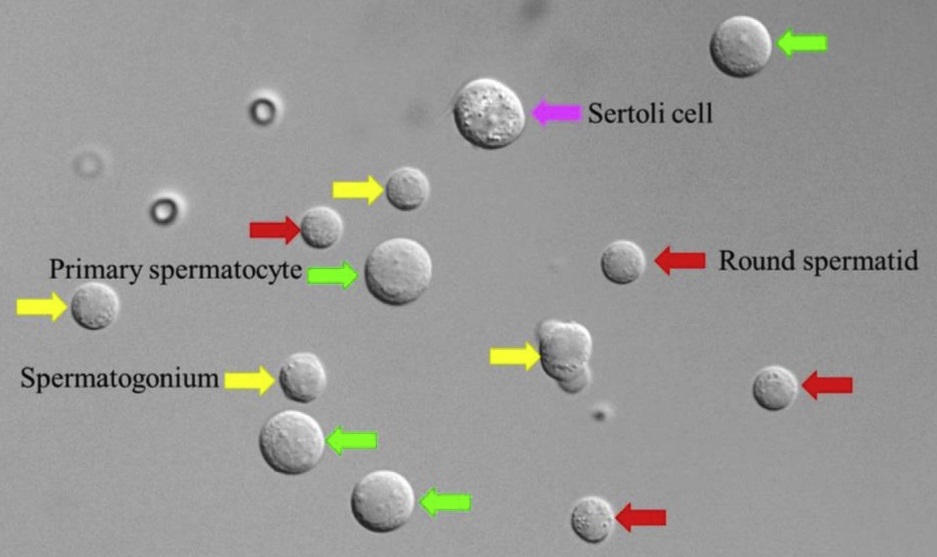
圖一、圖中紅色的箭頭是圓形精細胞(Round spermatid),黃色的箭頭是精原細胞(Spermatogonium),兩者之間長得非常像但是染色體一個是2N一個是1N,綠色的箭頭是初級精母細胞(Primary spermatocyte)是減數分裂之前也帶有2N的染色體,紫色箭頭則是Sertoli cell被稱為母細胞,主要功能是哺育成長中的精子細胞。
然而臨床上更嚴重的不孕狀況是男性患者為被診斷為造精功能異常,其精子無法完成減數分裂達到成熟階段,並停留在二倍體染色體的初級精母細胞階段(Primary spermatocyte)[3] (圖一)。在台灣,此類不孕症患者同常會被建議走向精子捐贈的療程。然而,2022年由日本團隊發表於EMBO report期刊的最新小鼠試驗發現利用顯微注射方式,將未成熟精子(初級精母細胞)置入處於減數分裂前期之原泡核期(germinal vesicle stage, GV stage)卵子中,經體外培養後,精、卵均可完成減數分裂而形成正常胚胎,唯其成功率極低且多數胚胎具異常之染色體數目。為改善此問題,近一步試驗發現將老鼠的卵母細胞的卵質減少,降低其體積至約1/2程度,可顯著提高生成具正常染色體受精卵的比率(圖二)。
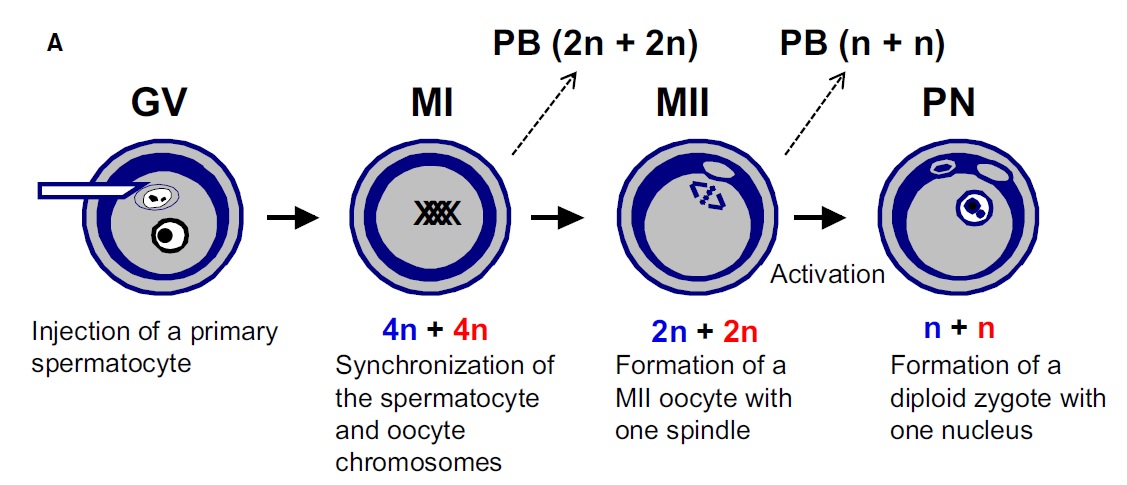
圖二、老鼠的GV stage卵母細胞注射進初級精母細胞,同步形成4n染色體,再同步進行第一次及第二次減數分裂後形成n+n的染色體,如同一般正常受精下的受精卵。
當使用正常大小的GV stage卵母細胞與初級精母細胞受精時,只有1% (1/96) 的胚胎可正常發育並產生子代,相比之下,當使用卵質減少的GV stage卵母細胞時,活產率明顯提升至19% (17/90) ,具近20倍的改善程度。且其中三隻公幼鼠長大達性成熟與正常母鼠交配後,已確認其具有生育能力(圖三)。
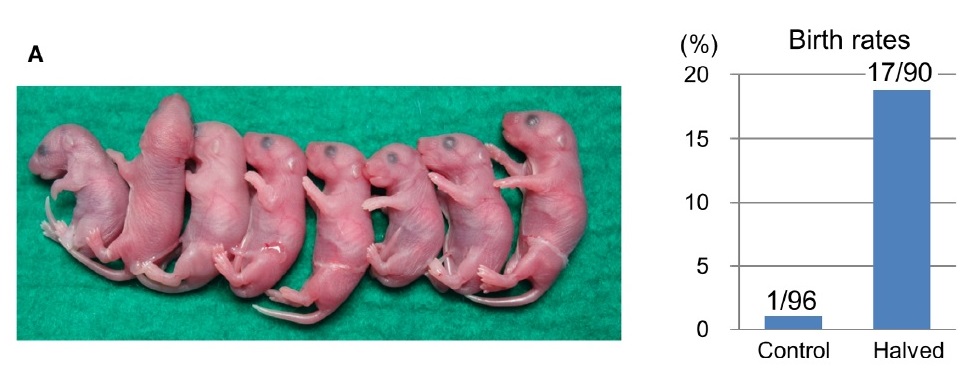
圖三、因此卵質的減少使注射精母細胞後的出生率上升。
臨床上男性若因減數分裂異常致使不孕發生,仍為極為棘手之案例,非常困難產生具患者血緣之後代。根據上述動物試驗結果可知,通過將卵質體積減少與顯微注射技術可顯著改善雙親減數分裂中的染色體分離錯誤,增加成功產生正常胚胎的可能性,雖仍須驗證於臨床使用之實際效益及安全性,該技術可能是治療嚴重男性不孕的替代策略[3]。
參考文獻:
- Kelli X. Gross, MD a*,Brent M. Hanson, MD b , James M. Hotaling, MD, FECSM c.Round Spermatid Injection. Urol Clin N Am 47 (2020) 175–183 https://doi.org/10.1016/j.ucl.2019.12.004 0094-0143/20/Published by Elsevier Inc.
- Hanson, B.M., Kohn, T.P., Pastuszak, A.W., Scott, R.T.Jr, Cheng, P.J., Hotaling, J.M. Round spermatid injection into human oocytes: a systematic review and meta-analysis. Asian J. Androl. 2021; 23: 363–369. doi: 10.4103/aja. aja_85_20
- Enguita-Marruedo A, Sleddens-Linkels E, Ooms M, de Geus V, Wilke M, Blom E, Dohle GR, Looijenga LHJ, van Cappellen W, Baart EB et al (2019) Meiotic arrest occurs most frequently at metaphase and is often incomplete in azoospermic men. FertilSteril 112: 1059 – 1070.e1053
圖片來源:
- Kelli X. Gross, MD a,*,Brent M. Hanson, MD b , James M. Hotaling, MD, FECSM. Round Spermatid Injection. Urol Clin N Am 47 (2020) 175–183 https://doi.org/10.1016/j.ucl.2019.12.004 0094-0143/20/Published by Elsevier Inc.
- Ogonuki N, Kyogoku H, Hino T, Osawa Y, Fujiwara Y, Inoue K, Kunieda T, Mizuno S, Tateno H, Sugiyama F et al (2022) Birth of mice from meiotically arrested spermatocytes following biparental meiosis in halved oocytes. EMBO Rep 23: e54992
其他相關訊息
-
18.Mar.2026
非多囊性卵巢症候群女性胰島素阻抗與體外受精結果之關聯性及metformin在改善效果
-
11.Feb.2026
從「棄用」到「救援」:重新定義混亂胚胎的價值






